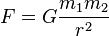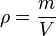Definisi umum dari basa adalah senyawa kimia yang menyerap ion hydronium ketika dilarutkan dalam air.Basa adalah lawan (dual) dari asam, yaitu ditujukan untuk unsur/senyawa kimia yang memiliki pH lebih dari 7. Kostik merupakan istilah yang digunakan untuk basa kuat. jadi kita menggunakan nama kostik soda untuk natrium hidroksida (NaOH) dan kostik postas untuk kalium hidroksida (KOH). Basa dapat dibagi menjadi basa kuat dan basa lemah. Kekuatan basa sangat tergantung pada kemampuan basa tersebut melepaskan ion OH dalam larutan dan konsentrasi larutan basa tersebut.
Sabtu, 13 Desember 2008
Asam
Berbagai definisi asam
Istilah "asam" merupakan terjemahan dari istilah yang digunakan untuk hal yang sama dalam bahasa-bahasa Eropa seperti acid (bahasa Inggris), zuur (bahasa Belanda), atau Säure (bahasa Jerman) yang secara harfiah berhubungan dengan rasa masam. Dalam kimia, istilah asam memiliki arti yang lebih khusus. Terdapat tiga definisi asam yang umum diterima dalam kimia, yaitu definisi Arrhenius, Brønsted-Lowry, dan Lewis.
- Arrhenius: Menurut definisi ini, asam adalah suatu zat yang meningkatkan konsentrasi ion hidronium (H3O+) ketika dilarutkan dalam air. Definisi yang pertama kali dikemukakan oleh Svante Arrhenius ini membatasi asam dan basa untuk zat-zat yang dapat larut dalam air.
- Brønsted-Lowry: Menurut definisi ini, asam adalah pemberi proton kepada basa. Asam dan basa bersangkutan disebut sebagai pasangan asam-basa konjugat. Brønsted dan Lowry secara terpisah mengemukakan definisi ini, yang mencakup zat-zat yang tak larut dalam air (tidak seperti pada definisi Arrhenius).
- Lewis: Menurut definisi ini, asam adalah penerima pasangan elektron dari basa. Definisi yang dikemukakan oleh Gilbert N. Lewis ini dapat mencakup asam yang tak mengandung hidrogen atau proton yang dapat dipindahkan, seperti besi(III) klorida. Definisi Lewis dapat pula dijelaskan dengan teori orbital molekul. Secara umum, suatu asam dapat menerima pasangan elektron pada orbital kosongnya yang paling rendah (LUMO) dari orbital terisi yang tertinggi (HOMO) dari suatu basa. Jadi, HOMO dari basa dan LUMO dari asam bergabung membentuk orbital molekul ikatan.
Walaupun bukan merupakan teori yang paling luas cakupannya, definisi Brønsted-Lowry merupakan definisi yang paling umum digunakan. Dalam definisi ini, keasaman suatu senyawa ditentukan oleh kestabilan ion hidronium dan basa konjugat terlarutnya ketika senyawa tersebut telah memberi proton ke dalam larutan tempat asam itu berada. Stabilitas basa konjugat yang lebih tinggi menunjukkan keasaman senyawa bersangkutan yang lebih tinggi.
Sistem asam/basa berbeda dengan reaksi redoks; tak ada perubahan bilangan oksidasi dalam reaksi asam-basa.
Sifat-sifat
Secara umum, asam memiliki sifat sebagai berikut:
- Rasa: masam ketika dilarutkan dalam air.
- Sentuhan: asam terasa menyengat bila disentuh, terutama bila asamnya asam kuat.
- Kereaktifan: asam bereaksi hebat dengan kebanyakan logam, yaitu korosif terhadap logam.
- Hantaran listrik: asam, walaupun tidak selalu ionik, merupakan elektrolit.
Sifat kimia
Dalam air, reaksi kesetimbangan berikut terjadi antara suatu asam (HA) dan air, yang berperan sebagai basa,
HA + H2O ↔ A- + H3O+
Tetapan asam adalah tetapan kesetimbangan untuk reaksi HA dengan air:
![K_a = \frac{[\mbox{H}_{3}\mbox{O}^+][ \mbox{A}^-]}{[\mbox{HA}]}](http://upload.wikimedia.org/math/4/7/5/475736351c84694f7cd757136735c907.png)
Asam kuat mempunyai nilai Ka yang besar (yaitu, kesetimbangan reaksi berada jauh di kanan, terdapat banyak H3O+; hampir seluruh asam terurai). Misalnya, nilai Ka untuk asam klorida (HCl) adalah 107.
Asam lemah mempunyai nilai Ka yang kecil (yaitu, sejumlah cukup banyak HA dan A- terdapat bersama-sama dalam larutan; sejumlah kecil H3O+ ada dalam larutan; asam hanya terurai sebagian). Misalnya, nilai Ka untuk asam asetat adalah 1,8 × 10-5.
Asam kuat mencakup asam halida - HCl, HBr, dan HI. (Tetapi, asam fluorida, HF, relatif lemah.) Asam-asam okso, yang umumnya mengandung atom pusat ber-bilangan oksidasi tinggi yang dikelilingi oksigen, juga cukup kuat; mencakup HNO3, H2SO4, dan HClO4. Kebanyakan asam organik merupakan asam lemah.
Larutan asam lemah dan garam dari basa konjugatnya membentuk larutan penyangga.
Sejarah
Sekitar tahun 1800, banyak kimiawan Prancis, termasuk Antoine Lavoisier, secara keliru berkeyakinan bahwa semua asam mengandung oksigen. Lavoisier mendefinisikan asam sebagai zat mengandung oksigen karena pengetahuannya akan asam kuat hanya terbatas pada asam-asam okso dan karena ia tidak mengetahui komposisi sesungguhnya dari asam-asam halida, HCl, HBr, dan HI. Lavoisier-lah yang memberi nama oksigen dari kata bahasa Yunani yang berarti "pembentuk asam". Setelah unsur klorin, bromin, dan iodin teridentifikasi dan ketiadaan oksigen dalam asam-asam halida ditemukan oleh Sir Humphry Davy pada tahun 1810, definisi oleh Lavoisier tersebut harus ditinggalkan.
Kimiawan Inggris pada waktu itu, termasuk Humphry Davy, berkeyakinan bahwa semua asam mengandung hidrogen. Kimiawan Swedia Svante Arrhenius lalu menggunakan landasan ini untuk mengembangkan definisinya tentang asam. Ia mengemukakan teorinya pada tahun 1884.
Pada tahun 1923, Johannes Nicolaus Brønsted dari Denmark dan Martin Lowry dari Inggris masing-masing mengemukakan definisi protonik asam-basa yang kemudian dikenal dengan nama kedua ilmuwan ini. Definisi yang lebih umum diajukan oleh Lewis pada tahun yang sama, menjelaskan reaksi asam-basa sebagai proses transfer pasangan elektron.
Penggunaan asam
Asam memiliki berbagai kegunaan. Asam sering digunakan untuk menghilangkan karat dari logam dalam proses yang disebut "pengawetasaman" (pickling). Asam dapat digunakan sebagai elektrolit di dalam baterai sel basah, seperti asam sulfat yang digunakan di dalam baterai mobil. Pada tubuh manusia dan berbagai hewan, asam klorida merupakan bagian dari asam lambung yang disekresikan di dalam lambung untuk membantu memecah protein dan polisakarida maupun mengubah proenzim pepsinogen yang inaktif menjadi enzim pepsin. Asam juga digunakan sebagai katalis; misalnya, asam sulfat sangat banyak digunakan dalam proses alkilasi pada pembuatan bensin.
teori atom
Teori atom dalam ilmu kimia dan fisika adalah teori mengenai sifat benda. Teori ini menyebutkan bahwa semua benda terbentuk dari atom-atom. Dasar filsafat untuk teori ini disebut atomisme. Teori ini dapat diterapkan pada semua fase umum benda seperti yang ditemukan di bumi, yaitu padat, cair, dan gas. Teori ini tidak dapat diterapkan pada plasma atau bintang neutron di mana terjadi lingkungan yang tidak standar, seperti suhu atau densitas ekstrim yang menghambat pembentukan atom.
faktor-faktor yang mempengaruhi laju reaksi
Faktor yang mempengaruhi laju reaksi
Laju reaksi dipengaruhi oleh beberapa faktor, antara lain:
Luas permukaan sentuh
Luas permukaan sentuh memiliki peranan yang sangat penting dalam laju reaksi, sebab semakin besar luas permukaan bidang sentuh antar partikel, maka tumbukan yang terjadi semakin banyak, sehingga menyebabkan laju reaksi semakin cepat. Begitu juga, apabila semakin kecil luas permukaan bidang sentuh, maka semakin kecil tumbukan yang terjadi antar partikel, sehingga laju reaksi pun semakin kecil. Karakteristik kepingan yang direaksikan juga turut berpengaruh, yaitu semakin halus kepingan itu, maka semakin cepat waktu yang dibutuhkan untuk bereaksi ; sedangkan semakin kasar kepingan itu, maka semakin lama waktu yang dibutuhkan untuk bereaksi.
Suhu
Suhu juga turut berperan dalam mempengaruhi laju reaksi. Apabila suhu pada suatu rekasi yang berlangusng dinaikkan, maka menyebabkan partikel semakin aktif bergerak, sehingga tumbukan yang terjadi semakin sering, menyebabkan laju reaksi semakin besar. Sebaliknya, apabila suhu diturunkan, maka partikel semakin tak aktif, sehingga laju reaksi semakin kecil.
Katalis
Katalis adalah suatu zat yang mempercepat laju reaksi kimia pada suhu tertentu, tanpa mengalami perubahan atau terpakai oleh reaksi itu sendiri. Suatu katalis berperan dalam reaksi tapi bukan sebagai pereaksi ataupun produk. Katalis memungkinkan reaksi berlangsung lebih cepat atau memungkinkan reaksi pada suhu lebih rendah akibat perubahan yang dipicunya terhadap pereaksi. Katalis menyediakan suatu jalur pilihan dengan energi aktivasi yang lebih rendah. Katalis mengurangi energi yang dibutuhkan untuk berlangsungnya reaksi.
Katalis dapat dibedakan ke dalam dua golongan utama: katalis homogen dan katalis heterogen. Katalis heterogen adalah katalis yang ada dalam fase berbeda dengan pereaksi dalam reaksi yang dikatalisinya, sedangkan katalis homogen berada dalam fase yang sama. Satu contoh sederhana untuk katalisis heterogen yaitu bahwa katalis menyediakan suatu permukaan di mana pereaksi-pereaksi (atau substrat) untuk sementara terjerat. Ikatan dalam substrat-substrat menjadi lemah sedemikian sehingga memadai terbentuknya produk baru. Ikatan atara produk dan katalis lebih lemah, sehingga akhirnya terlepas.
Katalis homogen umumnya bereaksi dengan satu atau lebih pereaksi untuk membentuk suatu perantarakimia yang selanjutnya bereaksi membentuk produk akhir reaksi, dalam suatu proses yang memulihkan katalisnya. Berikut ini merupakan skema umum reaksi katalitik, di mana C melambangkan katalisnya:
A + C → AC (1)
B + AC → AB + C (2)
Meskipun katalis (C) termakan oleh reaksi 1, namun selanjutnya dihasilkan kembali oleh reaksi 2, sehingga untuk reaksi keseluruhannya menjadi :
A + B + C → AB + C
Beberapa katalis yang pernah dikembangkan antara lain berupa katalis Ziegler-Natta yang digunakan untuk produksi masal polietilen dan polipropilen. Reaksi katalitis yang paling dikenal adalah proses Haber, yaitu sintesis amoniak menggunakan besi biasa sebagai katalis. Konverter katalitik yang dapat menghancurkan produk emisi kendaraan yang paling sulit diatasi, terbuat dari platina dan rodium.
jatuh bebas
Gerak jatuh bebas
Gerak jatuh bebas atau GJB adalah salah satu bentuk gerak lurus dalam satu dimensi yang hanya dipengaruhi oleh adanya gaya gravitasi. Variasi dari gerak ini adalah gerak jatuh dipercepat dan gerak peluru.
Secara umum gerak yang hanya dipengaruhi oleh gaya gravitasi memiliki bentuk:
di mana arti-arti lambang dan satuannya dalam SI adalah
- t adalah waktu (s)
- y adalah posisi pada saat t (m)
- y0 adalah posisi awal (m)
- v0 adalah kecepatan awal (m/s)
- g adalah percepatan gravitasi (m/s2)
Akan tetapi khusus untuk GJB diperlukan syarat tambahan yaitu:
sehingga rumusan di atas menjadi
Analogi gerak jatuh bebas
Apabila gerak jatuh bebas adalah gerak yang hanya dipengaruhi oleh gaya gravitasi, dapat dikemukakan gerak jatuh yang mirip akan tetapi tidak hanya oleh gaya gravitasi, misalnya gerak oleh gaya listrik.
| Gerak oleh gaya gravitasi | Gerak oleh gaya listrik | |
|---|---|---|
| Gaya |  |  |
| Percepatan |  | 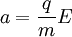 |
| Kecepatan |  |  |
| Posisi |  | 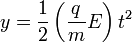 |
Dengan memanfaatkan kedua gaya yang mirip ini percobaan Millikan dilakukan untuk mengukur muatan elektron dengan menggunakan setetes minyak.
Gravitasi adalah gaya tarik-menarik yang terjadi antara semua partikel yang mempunyai massa di alam semesta. Fisika modern mendeskripsikan gravitasi menggunakan Teori Relativitas Umum dari Einstein, namun hukum gravitasi universal Newton yang lebih sederhana merupakan hampiran yang cukup akurat dalam kebanyakan kasus.
Sebagai contoh, Bumi yang memiliki massa yang sangat besar menghasilkan gaya gravitasi yang sangat besar untuk menarik benda-benda disekitarnya, termasuk makhluk hidup, dan benda benda yang ada di bumi. Gaya gravitasi ini juga menarik benda-benda yang ada diluar angkasa, seperti bulan, meteor, dan benda angkasa laiinnya, termasuk satelite buatan manusia.
Beberapa teori yang belum dapat dibuktikan menyebutkan bahwa gaya gravitasi timbul karena adanya partikel gravitron dalam setiap atom.
Hukum Gravitasi Universal Newton
Hukum gravitasi universal Newton dirumuskan sebagai berikut:
- Setiap massa titik menarik semua massa titik lainnya dengan gaya segaris dengan garis yang menghubungkan kedua titik. Besar gaya tersebut berbanding lurus dengan perkalian kedua massa tersebut dan berbanding terbalik dengan kuadrat jarak antara kedua massa titik tersebut.
- F adalah besar dari gaya gravitasi antara kedua massa titik tersebut
- G adalah konstanta gravitasi
- m1 adalah besar massa titik pertama
- m2 adalah besar massa titik kedua
- r adalah jarak antara kedua massa titik
Dalam sistem Internasional, F diukur dalam newton (N), m1 dan m2 dalam kilograms (kg), r dalam meter (m), dsn konstanta G kira-kira sama dengan 6,67 × 10−11 N m2 kg−2.
Dari persamaan ini dapat diturunkan persamaan untuk menghitung Berat. Berat suatu benda adalah hasil kali massa benda tersebut dengan percepatan gravitasi bumi. Persamaan tersebut dapat dituliskan sebagai berikut: W = mg. W adalah gaya berat benda tersebut, m adalah massa dan g adalah percepatan gravitasi. Percepatan gravitasi ini berbeda-beda dari satu tempat ke tempat lain.
massa jenis
Massa jenis adalah pengukuran massa setiap satuan volume benda. Semakin tinggi massa jenis suatu benda, maka semakin besar pula massa setiap volumenya. Massa jenis rata-rata setiap benda merupakan total massa dibagi dengan total volumenya. Sebuah benda yang memiliki massa jenis lebih tinggi (misalnya besi) akan memiliki volume yang lebih rendah daripada benda bermassa sama yang memiliki massa jenis lebih rendah (misalnya air).
Satuan SI massa jenis adalah kilogram per meter kubik (kg·m-3)
Massa jenis berfungsi untuk menentukan zat. Setiap zat memiliki massa jenis yang berbeda. Dan satu zat berapapun massanya berapapun volumenya akan memiliki massa jenis yang sama.
Rumus untuk menentukan massa jenis adalah
dengan
Satuan massa jenis dalam 'CGS [centi-gram-sekon]' adalah: gram per sentimeter kubik (g/cm3).
1 g/cm3=1000 kg/m3
Massa jenis air murni adalah 1 g/cm3 atau sama dengan 1000 kg/m3
Selain karena angkanya yang mudah diingat dan mudah dipakai untuk menghitung, maka massa jenis air dipakai perbandingan untuk rumus ke-2 menghitung massa jenis, atau yang dinamakan 'Massa Jenis Relatif'
Rumus massa jenis relatif = Massa bahan / Massa air yang volumenya sama